
技术文章
 更新时间:2025-08-27
更新时间:2025-08-27 点击次数:426
点击次数:426
成纤维细胞生长因子受体(FGFR)家族在细胞增殖、分化、血管生成和组织修复等关键生物学过程中扮演着核心角色。其中,FGFR2b作为FGFR2的一种异构体,因其在上皮细胞中的特异性表达和功能,成为癌症靶向治疗和再生医学研究的热点。FGFR2b抗体作为一种靶向治疗工具,通过特异性阻断FGFR2b信号通路,在抑制肿瘤生长、改善耐药性和调节微环境方面展现出巨大潜力。本文将从FGFR2b的生物学功能、抗体开发策略、临床应用现状及未来挑战等多个维度,全面探讨这一领域的研究进展。
FGFR2b是成纤维细胞生长因子受体2(FGFR2)的一种剪接变体,主要由上皮细胞表达,并与特定的配体(如FGF7、FGF10)结合后激活下游信号通路。FGFR2b的激活会触发RAS-MAPK、PI3K-AKT和STAT等关键信号级联反应,从而调控细胞的增殖、分化和生存。在正常生理状态下,FGFR2b信号通路对胚胎发育、组织修复和黏膜屏障的维持至关重要。例如,在皮肤和胃肠道上皮中,FGFR2b通过促进细胞更新和迁移,参与伤口愈合和屏障功能的调节。
然而,FGFR2b信号通路的异常激活与多种疾病密切相关,尤其是癌症。基因扩增、点突变或过度表达可能导致FGFR2b信号持续激活,驱动肿瘤的发生和发展。例如,在胃癌、乳腺癌和胆管癌中,FGFR2b的异常表达与肿瘤的侵袭性、转移和不良预后显著相关。此外,FGFR2b信号通路还参与肿瘤微环境的调节,通过影响免疫细胞浸润和血管生成,间接促进肿瘤进展。正因为其多方面的生物学功能,FGFR2b成为癌症治疗和再生医学中具吸引力的靶点。
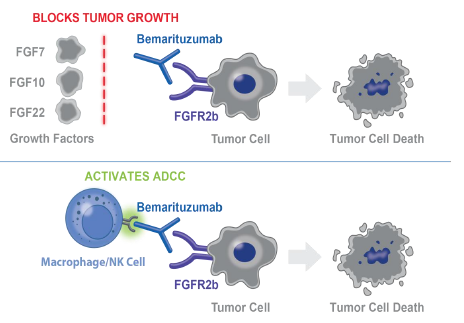
FGFR2b抗体的核心作用机制是通过特异性结合FGFR2b受体,阻断其与配体的相互作用,从而抑制下游信号通路的异常激活。这种靶向治疗策略具有高度特异性,能够最小化对正常细胞的毒性。目前,多种FGFR2b抗体(如bemarituzumab)已进入临床研究阶段,其作用机制主要包括以下几个方面:
首先,FGFR2b抗体通过空间位阻效应直接阻止配体(如FGF7和FGF10)与受体的结合。这种竞争性抑制使得FGFR2b无法二聚化和自磷酸化,从而中断MAPK和AKT等促生存信号的传导。其次,部分FGFR2b抗体还能诱导受体内存和降解,进一步降低细胞表面FGFR2b的密度,增强抑制效果。此外,一些工程化抗体(如双特异性抗体或抗体-药物偶联物)还通过募集免疫细胞或递送细胞毒性药物,实现多重抗肿瘤效应。
在肿瘤微环境调节方面,FGFR2b抗体可能通过抑制肿瘤相关成纤维细胞(CAF)和上皮细胞之间的串扰,减少促肿瘤因子的分泌。例如,临床前研究表明,阻断FGFR2b信号可以降低VEGF和IL-6等因子的表达,从而抑制血管生成和炎症反应。这种多模式的作用机制使得FGFR2b抗体不仅在单药治疗中表现出色,还能与化疗、免疫治疗等其他手段协同增效。
FGFR2b抗体在多种上皮源性癌症中展现出显著的治疗潜力,尤其是那些伴有FGFR2b过表达或基因扩增的恶性肿瘤。目前,研究最深入的领域包括胃癌、乳腺癌、胆管癌和非小细胞肺癌等。
在胃癌中,约10%的患者存在FGFR2b过表达或扩增,这与肿瘤的侵袭性和预后不良相关。II期临床试验(FIGHT研究)评估了bemarituzumab(一种人源化FGFR2b抗体)联合化疗一线治疗晚期胃癌的效果。结果显示,与单纯化疗相比,联合治疗显著延长了无进展生存期(PFS)和总生存期(OS),尤其是在FGFR2b高表达的患者亚组中,疗效更为突出。这一成果为FGFR2b抗体在胃癌中的临床应用提供了坚实证据。
在乳腺癌领域,三阴性乳腺癌(TNBC)和 luminal 型乳腺癌中均观察到FGFR2b的异常激活。临床前研究表明,FGFR2b抗体能够抑制肿瘤生长并逆转化疗耐药性。例如,在患者来源的异种移植(PDX)模型中,bemarituzumab单药或与紫杉醇联用,显著减少了肿瘤体积并降低了转移风险。类似的结果也在胆管癌和非小细胞肺癌中得到验证,尤其是那些伴有FGFR2基因融合或扩增的亚型。
此外,FGFR2b抗体在罕见癌症(如唾液腺癌和卵巢癌)中也有个案报道。这些研究提示,FGFR2b可能是一个跨多种肿瘤类型的广谱靶点,而基于生物标志物的患者筛选将是未来临床开发的关键。
尽管FGFR2b抗体在早期临床试验中表现出 promising 的结果,但其临床应用仍面临多重挑战。首先,患者筛选是一大难题。目前,FGFR2b过表达或基因扩增的检测依赖于免疫组化(IHC)或荧光原位杂交(FISH),但这些方法的标准化和灵敏度仍需优化。例如,肿瘤异质性可能导致假阴性结果,而低水平FGFR2b表达的患者可能无法从治疗中获益。
其次,耐药性是FGFR2b抗体治疗的主要障碍。耐药机制包括:1)下游信号通路的代偿性激活,如EGFR或HER2信号的上调;2)FGFR2基因的二次突变,导致抗体结合亲和力下降;3)肿瘤微环境的适应,例如CAF分泌替代性生长因子(如FGF1或FGF3),绕过FGFR2b的阻断。为了解决这些问题,联合治疗策略正在积极探索中,例如FGFR2b抗体与MEK抑制剂、免疫检查点抑制剂或化疗药物的组合。
安全性也是不可忽视的挑战。FGFR2b在正常组织(如皮肤和角膜)中的生理功能可能导致靶向毒性。临床试验中,部分患者出现高磷血症、干眼症或皮肤干燥等不良反应,这要求临床医生在疗效和毒性之间找到平衡。新一代抗体通过工程化改造(如降低Fc效应子功能或增加肿瘤选择性)有望改善安全性问题。
未来研究将从多个方向拓展FGFR2b抗体的应用前景。首先,基于生物标志物的精准医疗是核心方向。除了传统的IHC和FISH,液体活检和转录组学分析可能帮助识别更广泛的患者群体。例如,循环肿瘤DNA(ctDNA)检测可用于动态监测FGFR2b扩增状态,预测治疗响应和耐药演变。
其次,新型抗体格式的开发将增强治疗效能。双特异性抗体(如同时靶向FGFR2b和PD-L1)能够协同调节肿瘤细胞和免疫微环境;抗体-药物偶联物(ADC)则通过定向递送细胞毒性药物,提高杀伤效率并降低系统毒性。此外,纳米抗体和CAR-T细胞疗法的探索也为FGFR2b靶向治疗提供了新思路。联合治疗策略的优化是另一重点。临床前数据表明,FGFR2b抗体与免疫检查点抑制剂(如抗PD-1抗体)联用,可通过调节T细胞浸润和抑制免疫抑制微环境,实现协同抗肿瘤效果。多项临床试验(如bemarituzumab与pembrolizumab联用)正在进行中,初步结果令人期待。最后,FGFR2b抗体在非肿瘤领域(如组织再生和纤维化疾病)的应用也值得关注。例如,在肺纤维化或肝硬化模型中,FGFR2b信号通路的过度激活与病理进展相关,而抗体阻断可能缓解纤维化过程。这为FGFR2b靶向治疗开辟了更广阔的应用场景。
成纤维细胞生长因子受体2b抗体代表了一种具有高度特异性和多模式作用机制的靶向治疗工具。从基础研究到临床转化,其在胃癌、乳腺癌等多种癌症中展现出显著疗效,同时也面临患者筛选、耐药性和安全性等挑战。未来,通过精准医疗、新型抗体开发和联合策略优化,FGFR2b抗体有望不仅改善癌症患者的生存预后,还可能拓展至非肿瘤领域。这一领域的持续创新将为精准医疗时代提供更多突破性治疗方案。

杭州斯达特 志在为全球生命科学行业提供优质的抗体、蛋白、试剂盒等产品及研发服务。依托多个开发平台:重组兔单抗、重组鼠单抗、快速鼠单抗、重组蛋白开发平台(E.coli,CHO,HEK293,InsectCells),已正式通过欧盟98/79/EC认证、ISO9001认证、ISO13485。
成纤维细胞生长因子受体2b抗体:从基础研究到临床转化的前沿探索